|
| Solutions
aqueuses de chlorure de sodium | Masse volumique
| Concentration massique | Récapitulatio
|
|
Pour utiliser utilement cette page vous devez être en possession
de vos résultats expérimentaux
|
| |
|
|
|
La concentration est la grandeur qui caractérises
la quantité de soluté mise en solution par un solvant.
|
|
|
| |
1.1. Peser la masse de chlorure de sodium.
|
 |
|
j
|
Poser un bécher propre et sec sur la balance
|
|
k
|
En appuyant sur le bouton «Tare», la balance affiche : 0,00 g.
|
|
l
|
A l'aide d'une spatule, verser lentement le sel de cuisine, jusqu'à
ce que la masse affichée soit (à 0,1 g près) la masse désirée
:
|
|
|
|
|
| |
1.2. Préparer la solution. |
 |
|
j
|
La fiole jaugée est tarée avant d'introduire le
sel
|
|
k
|
La fiole jaugée est remplie en partie d'eau avant d'introduire
le sel.
|
|
l
|
Agiter la fiole bouchée assez longtemps pour dissoudre tout le
sel.
|
|
m
|
A l'aide d'une pissette, apporter l'eau en quantité suffisante
pour ajuster le ménisque au niveau du trait de jauge
|
| |
|
|
Sur les préparations pharmaceutiques on peut lire fréquemment
: «q.s.p. ..... pour 100 mL» ce qui signifie «quantité suffisante
pour obtenir 100 mL de solution», et non pas qu'il faut
dissoudre le soluté dans 100 mL de solvant
|
|
|
n
|
La fiole est bouchée à nouveau et agitée pour homogénéiser le
mélange
|
|
o
|
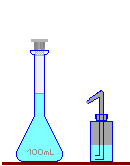
Le niveau est vérifié une dernière fois.
|
|
p
|
Puis la fiole est pesée pour calculer la masse volumique
|
|
 |
|
|
|
|
|
|
Les solutions ont toutes le même volume, ce qui les différentie
est la masse de soluté dissoute. On préfère substituer à la masse
volumique la concentration (massique volumique) définie comme
suit :
|
| |
Ce qu'il faut retenir
...
|
|
|
|
La concentration est la masse de soluté dissoute dans la quantité
de solvant nécessaire pour obtenir un litre de solution.
|
|
|
|
|
|
Chaque groupe rapporte sa solutions pour comparaison.
|
 |
|
|
| |
Toute les solutions sont incolores et ne peuvent être classé
par leur aspect
|
| |
Dans une fiole au moins il reste du sel que malgré tout
n'a pu être dissout
|
| |
Il existe donc une limite au delà de laquelle toutes les
solutions ont même concentration. On dit alors que la solution
est saturée.
|
| |
On appelle limite de solubilité la concentration de la
solution saturée
|
|
|
Récapitulation
|
|
| |
| Groupe |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
| m
en g |
|
|
|
|
|
|
|
|
|
|
| V
en L |
0,1 |
0,1 |
0,1 |
0,1 |
0,1 |
0,1 |
0,1 |
0,1 |
0,1 |
0,1 |
| µ
g/cm3 |
|
|
|
|
|
|
|
|
|
|
| C
g/L |
|
|
|
|
|
|
|
|
|
|
|
| |
|
© Villafruela Daniel
mise à jour le
20-12-2002
|
|
|
|
|
|
|
|
|
|